Numere cuantice
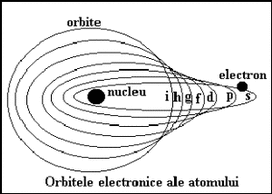
1. Numarul cuantic principal n determina numarul straturilor electronice. Electronii cu acelasi numar cuantic principal se gasesc la aceeasi distanta de nucleu formand un strat electronic.
Numarul cuantic principal poate avea valorile n = 1, 2, 3, 4, 5, 6 si 7 care se numesc stratul K, L, M, N, O, P si Q.
Stratul n=1 se numeste stratul electronic K care se afla cel mai aproape de nucleul atomic si are nivelul energetic cel mai mic. Cu cat valorile lui n sunt mai mari, cu atat stratul se afla la o distanta mai mare de nucleu, legatura dintre electronii existenti din acel strat si nucleul atomului este mai slaba.
2. Numarul cuantic secundar determina substraturile electronice, adica orbitele si forma lor care poate fi circulara sau eliptica.
Valorile lui l depinde de valoarea corespunzatoare a lui n, iar l poate avea valorile 0, 1, 2, 3,...n - l, deoarece intre numere cuantice n si l exista relatia l = n - 1.
De exemplu, pentru stratul M determinat de numarul cuantic principal n = 3, vom avea trei substraturi electronice pentru care l are valorile 0, l si 2. Cu cat lare valoarea mai mica cu atat orbita sa eliptica este mai alungita, la valoarea maxima a lui l, adica l = n - l, elipsa se transforma in cerc.
3. Numarul cuantic magnetic m determina pozitia spatiala (orientarea in spatiu) a planului orbitelor electronice. El poate avea toate valorile intregi negative si pozitive cuprinse intre - l si + l:
-l,...-2, -1, 0, +1, +2,...+l
De exemplu; l = 0; m = 0;
/ = l ; m = - l, 0, + l;
l = 2; m = -2, -1, 0, + l, + 2.
4. Numarul cuantic al spinului s se datoreste miscarii electronului in jurul propriei sale axe, miscare numita spin electronic care da nastere unui moment magnetic propriu al electronului.
Deoarece relatia electronului in jurul axei sale nu se poate face decat in doua sensuri, numarul cuantic al spinului s nu poate avea decat doua valori: +1/2 sau - 1/2, dupa cum sensul rotatiei electronului este paralel sau antiparalel cu acela al rotirii orbitei electronice.
Tinand seama de valorile pe care le pot lua cele 4 numere cuantice n, l, m, s si de principiul de excluziune a lui Pauly care spune ca, "intr-un atom nu pot exista doi electroni care sa aiba toate cele 4 numere cuantice identice" sau cei doi electroni care apartin aceluiasi atom aflati pe o orbita electronica, se deosebesc intre ei, cel putin printr-unul din cele 4 numere cuantice. Numarul maxim de electroni N ce pot exista intr-un strat cu numarul cuantic principal n este dat de relatia: N = 2n2
Electroni cu numarul cuantic principal n = 1 constituie stratul K, iar cel cu numarul cuantic principal n = 2 stratul L .
Numarul maxim de electroni dintr-un substrat cu numarul cuantic secundar l este dat de relaœia: 2(2l + 1).
Din cele prezentate se observa ca, diferitele straturi si substraturi electronice corespunzatoare numerelor cuantice principale n si secundare l vor contine, incepand de la nucleu (stratul K) spre periferie (stratul Q), numarul maxim de electroni.
Numarul maxim de electroni pe straturi: n - 1 2 3 4 5 6 7
strat - K L M N O P Q..........N=2n2 - 2 8 18 32 50 72 98
Numarul maxim de electroni pe substraturi: - 0 1 2 3 4 5 6
substrat - s p d f g h i
N=2(2l+1) - 2 6 10 14 18 22 26
In fizica atomica notarea substratului electronic l = 0, avand 2 electroni se face cu litera mica s, substraturile cu 6, 10, 14, 18, 22, 26 electroni, adica substraturile l = 1, 2, 3, 4, 5, 6 cu literele p, d, f, g, h, i.
Fiecare strat de electroni este format din substraturi, iar substraturile sunt alcatuite din una sau mai multe orbite, intre care exista diferente de energie.
Orbitele sunt de sapte feluri si se noteaza cu literele mici s, p, d, f, g, h, i. Orbitele de acelasi tip formeaza un substrat. Intr-un strat de electroni pot exista cel mult sapte feluri de substraturi corespunzator celor sapte tipuri de orbite.
Numarul cuantic principal poate avea valorile n = 1, 2, 3, 4, 5, 6 si 7 care se numesc stratul K, L, M, N, O, P si Q.
Stratul n=1 se numeste stratul electronic K care se afla cel mai aproape de nucleul atomic si are nivelul energetic cel mai mic. Cu cat valorile lui n sunt mai mari, cu atat stratul se afla la o distanta mai mare de nucleu, legatura dintre electronii existenti din acel strat si nucleul atomului este mai slaba.
2. Numarul cuantic secundar determina substraturile electronice, adica orbitele si forma lor care poate fi circulara sau eliptica.
Valorile lui l depinde de valoarea corespunzatoare a lui n, iar l poate avea valorile 0, 1, 2, 3,...n - l, deoarece intre numere cuantice n si l exista relatia l = n - 1.
De exemplu, pentru stratul M determinat de numarul cuantic principal n = 3, vom avea trei substraturi electronice pentru care l are valorile 0, l si 2. Cu cat lare valoarea mai mica cu atat orbita sa eliptica este mai alungita, la valoarea maxima a lui l, adica l = n - l, elipsa se transforma in cerc.
3. Numarul cuantic magnetic m determina pozitia spatiala (orientarea in spatiu) a planului orbitelor electronice. El poate avea toate valorile intregi negative si pozitive cuprinse intre - l si + l:
-l,...-2, -1, 0, +1, +2,...+l
De exemplu; l = 0; m = 0;
/ = l ; m = - l, 0, + l;
l = 2; m = -2, -1, 0, + l, + 2.
4. Numarul cuantic al spinului s se datoreste miscarii electronului in jurul propriei sale axe, miscare numita spin electronic care da nastere unui moment magnetic propriu al electronului.
Deoarece relatia electronului in jurul axei sale nu se poate face decat in doua sensuri, numarul cuantic al spinului s nu poate avea decat doua valori: +1/2 sau - 1/2, dupa cum sensul rotatiei electronului este paralel sau antiparalel cu acela al rotirii orbitei electronice.
Tinand seama de valorile pe care le pot lua cele 4 numere cuantice n, l, m, s si de principiul de excluziune a lui Pauly care spune ca, "intr-un atom nu pot exista doi electroni care sa aiba toate cele 4 numere cuantice identice" sau cei doi electroni care apartin aceluiasi atom aflati pe o orbita electronica, se deosebesc intre ei, cel putin printr-unul din cele 4 numere cuantice. Numarul maxim de electroni N ce pot exista intr-un strat cu numarul cuantic principal n este dat de relatia: N = 2n2
Electroni cu numarul cuantic principal n = 1 constituie stratul K, iar cel cu numarul cuantic principal n = 2 stratul L .
Numarul maxim de electroni dintr-un substrat cu numarul cuantic secundar l este dat de relaœia: 2(2l + 1).
Din cele prezentate se observa ca, diferitele straturi si substraturi electronice corespunzatoare numerelor cuantice principale n si secundare l vor contine, incepand de la nucleu (stratul K) spre periferie (stratul Q), numarul maxim de electroni.
Numarul maxim de electroni pe straturi: n - 1 2 3 4 5 6 7
strat - K L M N O P Q..........N=2n2 - 2 8 18 32 50 72 98
Numarul maxim de electroni pe substraturi: - 0 1 2 3 4 5 6
substrat - s p d f g h i
N=2(2l+1) - 2 6 10 14 18 22 26
In fizica atomica notarea substratului electronic l = 0, avand 2 electroni se face cu litera mica s, substraturile cu 6, 10, 14, 18, 22, 26 electroni, adica substraturile l = 1, 2, 3, 4, 5, 6 cu literele p, d, f, g, h, i.
Fiecare strat de electroni este format din substraturi, iar substraturile sunt alcatuite din una sau mai multe orbite, intre care exista diferente de energie.
Orbitele sunt de sapte feluri si se noteaza cu literele mici s, p, d, f, g, h, i. Orbitele de acelasi tip formeaza un substrat. Intr-un strat de electroni pot exista cel mult sapte feluri de substraturi corespunzator celor sapte tipuri de orbite.
