Invelisul electronic al atomului este alcatuit din electroni care sunt asezati si se rotesc pe orbite electronice situate la exteriorul nucleului atomic.
Pentru a explica modul de asezare a electronilor in jurul nucleului, cum si spectrul de linii (discontinuu) dat de atomii diferitelor elemente, Niels Bohr, folosind modelul atomului planetar al lui Rutherford si teoria cuantelor a lui Plank, formuleaza in 1913 trei postulate:
-miscarea electronului in jurul nucleului se face numai pe anumite orbite, stationare sau permise care corespund unor energii cuantificate a atomului
- in cursul miscarii electronului pe o orbita permisa, atomul isi conserva energia sa totala, adica nu absoarbe si nu emite energie
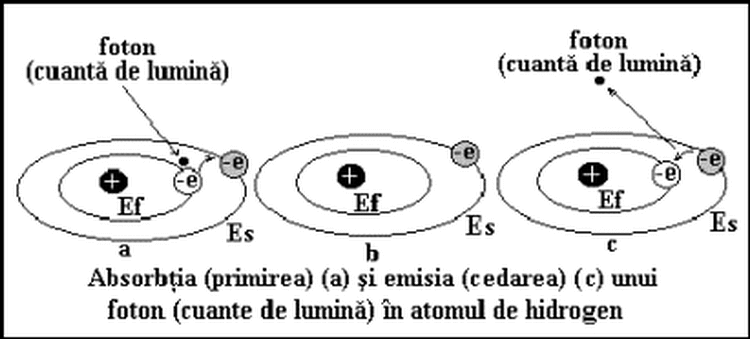
- absorbtia sau emisia de energie luminoasa are loc numai la salturile electronului de pe orbita inferioara pe una superioara si la revenirea lui inapoi.
Electronii au energie si masa.
Acestea pot fi, constante atunci electronul se gaseste pe orbita fundamentala, sau poate creste prin absorbtia unui foton din exteriorul atomului si atunci acesta va trece pe o orbita superioara.
-fotonul electronic - acest foton este o particula neutra din punct de vedere electric si se numeste foton electronic care arata starea de excitatie a atomului. Electronul aflat pe aceasta orbita, nu are o situatie stabila si va reveni pe orbita fundamentala, eliberand fotonul electronic si energia primita.
Odata cu emiterea acestui foton electronic atomul trece din starea de excitatie in starea fundamentala.
Variatia energiei dintre cele doua stari este data de relatia DE = Ey - Ei = hn.
Pentru a explica modul de asezare a electronilor in jurul nucleului, cum si spectrul de linii (discontinuu) dat de atomii diferitelor elemente, Niels Bohr, folosind modelul atomului planetar al lui Rutherford si teoria cuantelor a lui Plank, formuleaza in 1913 trei postulate:
-miscarea electronului in jurul nucleului se face numai pe anumite orbite, stationare sau permise care corespund unor energii cuantificate a atomului
- in cursul miscarii electronului pe o orbita permisa, atomul isi conserva energia sa totala, adica nu absoarbe si nu emite energie
- absorbtia sau emisia de energie luminoasa are loc numai la salturile electronului de pe orbita inferioara pe una superioara si la revenirea lui inapoi.
Electronii au energie si masa.
Acestea pot fi, constante atunci electronul se gaseste pe orbita fundamentala, sau poate creste prin absorbtia unui foton din exteriorul atomului si atunci acesta va trece pe o orbita superioara.
-fotonul electronic - acest foton este o particula neutra din punct de vedere electric si se numeste foton electronic care arata starea de excitatie a atomului. Electronul aflat pe aceasta orbita, nu are o situatie stabila si va reveni pe orbita fundamentala, eliberand fotonul electronic si energia primita.
Odata cu emiterea acestui foton electronic atomul trece din starea de excitatie in starea fundamentala.
Variatia energiei dintre cele doua stari este data de relatia DE = Ey - Ei = hn.
|
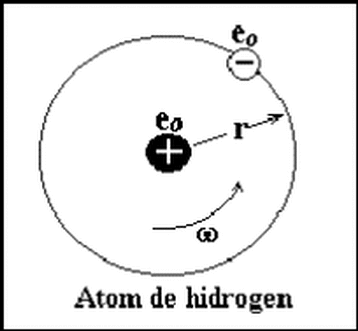
Atomul de hidrogen are un singur electron, intre acesta si nucleu exista o forta de atractie electrostatica a carei intensitate este prezentata in ecuatia 1, iar pentru ca electronul sau sa nu cada pe nucleu exista o forta centrifuga 2 care este egala cu forta de atractie electrostatica, de unde rezulta ecuatia 3.
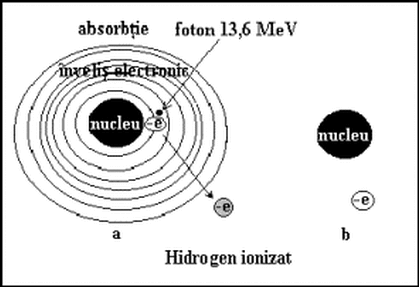
Actiunea electronului care se roteste pe orbita in miscare de revolutie, mor2w2p, este egala cu un multiplu al lui h, adica ecuatia mor2w2p = nh, unde n = 1,2,3.... Ridicam la patrat ecuatia si o impartim la ecuatia de mai sus si obtinem ecuatia 4, de unde rezulta ca, razele orbitelor atomului de hidrogen 5 sunt proportionale cu patratele numerelor intregi 1, 4, 9, 16,... (Tabelul 1a). Electronul care se roteste pe o orbita are, pe de o parte energie cinetica 6, unde membrul din dreapta este egal cu ecuatia 7, iar pe de alta parte contine si energie potentiala 8 care este negativa, deoarece in timpul caderii sale pe o orbita mai apropiata de nucleu, electronul pierde energie pe care o cedeaza in exterior. In cazul acesta, energia totala este 9, unde introducem valoarea lui r si obtinem valoarea electronului pe orbita n, 10. Daca electronul cade de pe o orbita superioara m, pe una inferioara n, atunci se elibereaza diferenta de energie Em - En = hn si deci, frecventa energiei emise este conform ecuatiei 11. Fractia din fata parantezei contine numai marimi constante, de unde se obtine constanta lui Rydberg, R = 3,288 . 1015Hz. In final rezulta ecuatia 12 care reprezinta frecventa si toata lungimea de unda emisa de atom si frecventa luminii care este absorbita de atom. Daca atomului de hidrogen ii furnizam suficienta energie din exterior, el poate emite o parte a spectrului de radiatii electromagnetice si anume: radiatii hertiene, radiatii termice care se impart in radiatii infrarosii, vizibile si ultraviolete (Tabelul 1b), iar daca acestuia ii furnizam energia hn = 21,78 . 10-12 erg, adica, 13,6 eV, cu ajutorul unui fascicul de fotoni ultravioleti sau nucleari g sau X, atunci atomul pierde electronul si devine ion pozitiv, protonul si electronul devin liberi. Sommerfeld (1916) dezvoltand teoria lui Bohr, considera ca electronul se poate roti nu numai pe orbite circulare, dar si pe orbite eliptice, nucleul atomic gasindu-se intr-unul din cele dou“ focare ale elipsei. Electronii rotindu-se in jurul nucleului, au dupa mecanica cuantica sau ondulatorie, atat proprietati de particula cat si de unda, ceea ce le confera anumite functii de unda orbitale. |